Intresset för att utbilda sig inom det farmacevtiska området har fortsatt varit lågt trots att efterfrågan efter personal spås öka än mer. Redan idag är det på många håll brist på personal med farmaceutisk utbildning. Många kommer dessutom att gå i pension de närmaste åren.
Månads arkivering mars 2013
Kampanj för apoteksutbildning
Paracetamol är fortsatt störst
Mer än en miljon svenskar hämtade ut paracetamol på recept förra året. Jämfört med 2011 är det en ökning med nästan fem procent (4,9) vilket gör substansen till det mest förskrivna läkemedlet. Å andra sidan har förskrivningen av diklofenak minskat betydligt mellan de två åren, med drygt tolv procent. Det framgår av Socialstyrelsens läkemedelsstatistik för 2012.
Inget prövningstillstånd för TLV
För ett drygt år sedan sade Tandvårds- och läkemdelsförmånsverket att det återbäringsavtal som Region Skåne träffat med företaget UCB om TNF-hämmaren Cimzia stred mot lagen om läkemedelsförmåner.
Det beslutet överklagades av Region Skåne till Förvaltningsrätten varpå TLV förbjöd samarbetena att fortsätta till dess att frågan är avgjord i domstol. När förvaltningsrätten valde att frysa TLVs förbund vände sig myndigheten till Kammarrätten i Stockholm.
Kammarrätten har nu meddelat att de inte kommer att pröva frågan och Region Skåne kan därmed fortsätta med prisöverenskommelser tills dess att förvaltningsrätten har avgjort frågan.
Svenskar köper antibiotika illegalt
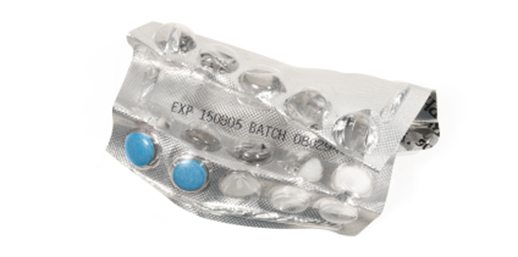
Under en vecka under hösten 2012 agerade 100 länder gemensamt för att komma till rätta med handel av olagliga läkemedel. Operationen som går under namnet Pangea V samordnas av Interpol och resultaten av den svenska delen av operationen redovisas nu av Läkemedelsverket.
Totalt kontrollerade Läkemedelsverket i samarbete med Tullverket 556 post- och kurirförsändelser varav 55 beslagtogs. Analyser av 74 produkter har analyserats och totalt har 32 annonser för läkemedel tagits bort från sajter där de säljs.
Många av försändelserna som beslagtogs innehöll lösa kapslar packade i plastpåsar utan någon information om vad det innehöll.
– Här ser vi en direkt risk då det inte finns någon identitet på tabletterna. Som konsument vet du inte vad du får eller hur de fungerar, säger Ingela Ottosson, utredare på Läkemedelsverket i ett pressmeddelande.
Bland de olagliga läkemedlen som beslagtogs var 21 procent inom området värk, 12 procent var antibiotika, 11 procent doping och 9 procent bantingspreparat. De vanligaste avsändarländerna var Thailand, Indien och Turkiet.
– Använder du antibiotika på fel sätt kan du vara med och bidra till resistensutvecklingen. Det är inte bara allvarligt för dig utan påverkar hela vårt samhälle, säger Ingela Ottosson.
Brist på viktiga läkemedel upprör
Den 8 mars, en fredag eftermiddag, kom information om att en bristsituation för Adrenalin 1 mg/ml (epinefrin) från Mylan skulle uppstå på måndagen. Att uppgifter om restnoteringar kommer med kort varsel förekommer trots att företagen egentligen ska informera om detta minst två månader i förväg. Men att beskedet för ett livsviktigt läkemedel kommer så sent innan en helg är upprörande menar läkaren Daniel Carlzon, klinisk farmakolog vid Sahlgrenska universitetssjukhuset.
– Adrenalin är ett läkemedel som används inom akutsjukvården och som bland annat finns i akutväskor i sjukvården. Att få besked om en restnotering med så kort framförhållning är inte bra och kan skapa oro och allvarliga problem i vården, säger han.
Epinefrin i dosen 1 mg/ml för injektion finns inte i någon annan registrerad produkt på den svenska marknaden. Mylan, som marknadsför produkten har importerat en annan adrenalinprodukt i form av Adrenalin Galenica 1mg/ml så att en brist inte ska uppstå. Den kan bara förskrivas på licens och för att underlätta för vården kommer Läkemedelsverket att bevilja kliniklicenser, just för att det rör sig om ett livsviktigt läkemedel.
– Men det ska trots allt göras en ansökan som ska handläggas vilket tar tid. Jag hade önskat att Läkemedelsverket hade bättre framförhållning för den här typen av meddelanden så att sjukvården hinner förbereda sig. Framförallt när informationen kommer sent en fredagseftermiddag, säger Daniel Carlzon.
I det aktuella fallet lade Läkemedelsverket ut informationen på sin hemsida och på bland annat Twitter. De har därefter också skickat brev till akutmottagningar, hjärtavdelningar, operationsavdelningar och till sjukhusapotek. Företaget Mylan har meddelat myndigheten att de avsåg att skicka brev till sjukvården den 12 mars.
Både vård och apotek behöver få reda på bristsituationer i god tid för att på ett bra sätt kunna planera sitt arbete. Och det är inte alltid som företagen är bra på att informera säger Kerstin Claesson, utredare på Läkemedelsverket.
– De skiljer det sig åt, ibland är företagen proaktiva men ibland måste vi uppmana dem att agera. Vi har inte heller någon juridisk rätt eller skyldighet att kontrollera vad det är för information som de skickar utan det bygger på att de vill informera oss, säger hon.
Enligt en enkät som Lif skickat ut till sina medlemsföretag uppger 22 av 30 företag att de haft restnoterade läkemedel under 2011 och 2012. Enligt regelverket ska företaget som har ett läkemedel godkänt anmäla en permanent eller tillfällig brist två månader innan det inträffar. Men det görs långt ifrån alltid enligt Läkemedelsverket.
– Det är stor variation på hur långt innan vi får information det kan vara en månad i förväg eller mindre. I fallet med Adrenalin från Mylan fick vi beskedet kort annan vi gick ut med informationen på fredagen. Tyvärr har vi inga möjligheter att komma med några rättsligt bindande förelägganden i den här frågan, säger Kerstin Claesson.
På Mylan säger man att man arbetar tillsammans med sin underleverantör för att lösa problemet.
Restnoteringar vanligt bland företagen
Restnoteringar och brist av läkemedel har uppmärksammats av fler aktörer på läkemedelsmarknaden och uppges vara ett växande problem. Fenomenet har bland annat diskuterats i samband med apoteks- och läkemedelsutredningen. De forskande läkemedelsföretagens branschorganisation Lif har nu försökt kartlägga problemet och i december skickade de ut en enkätundersökning till sina medlemmar för att undersöka hur vanligt detta är.
Totalt svarade 30 företag på enkäten. 22 av dessa uppger att de haft restnoterade läkemedel under åren 2011 och 2012. Vanligast är att företagen haft mellan en och fyra restnoteringar men det finns ett fåtal företag som haft en betydligt större andel. Lif tror att en förklaring till det kan vara att de restnoterat på förpackningsnivå istället för produktnivå som efterfrågades.
Av de 22 företagen som uppgav restnoteringar hade 12 haft unika noteringar alltså produkter som inte tillhör någon utbytesgrupp eller kritiska restnoteringar som innebär hälsorisker för patienten om inte tillgången till läkemedlet säkras. Tre av unika eller kritiska restnoteringarna varade längre än tre månader och majoriteten varade upp till en månad.
Enligt enkäten kontaktar företagen apoteken ”nästan alltid” och i 83 procent kontaktas distributören då restnoteringar uppstår.
Lif skriver i sin rapport att läkemedelsföretagen lättare vill kunna använda nordiska förpackningar för att kunna minska risken för restnoterade läkemedel. I enkäten framkommer också att det saknas bra kanaler för informationsspridning när en restsituation uppstår.
Så ska apotekens roll bli tydligare
För snart två år sedan kom den svenska versionen av vad som är god kvalitet för apotekskunder, Good Pharmacy Practice. Det svenska GPP-dokumentet som togs fram av Apotekarsocieteten och Sveriges apoteksförening ska användas när Läkemedelsverket på uppdrag av socialdepartementet nu tar fram och utvecklar nationella indikatorer för god patientsäkerhet, tillgänglighet och kvalitet på apotek.
Med nationella indikatorer är det meningen att allmänheten ska ha ett underlag för att jämföra apoteken.
– Det är jättebra att man i arbetet med indikatorerna tar avstamp i det dokument som branschen själv ser som viktigt, säger apotekaren Annika Nordén Hägg som är en av dem som tagit fram det svenska GPP-dokumentet.
– Det blir en kvalitetsstämpel på att apoteken är en del av hälso- och sjukvården. Det är alldeles utmärkt.
Sommaren 2014 ska arbetet med de nationella indikatorerna vara klart. I den nationella läkemedelstrategin konstaterades i analysen 2012 att apoteksaktörernas roll behövde göras tydligare. Beslutet om de nationella indikatorerna är en del i det tydliggörandet.
Det är också det andra uppdraget som Läkemedelsverket fått och som har sin upprinnelse i den nationella läkemedelsstrategin; strukturerade läkemedelssamtal. Tanken så som det formuleras i regeringsbeslutet är att läkare ska remittera patienter till läkemedelssamtalen och att ”farmacevterna ska återrapportera utfallet”.
Regeringen vill att försöksverksamheten inskränks till en avgränsad patientgrupp med dålig följsamhet och att försöket utvärderas. Utvärderingen ska vara klar den 15 december 2014.
Fler tvångslicenser att vänta
Undantaget i handelsavtalet TRIPS som gör det möjligt att upphäva ett läkemedelspatent och starta egen tillverkning av läkemedlet genom en så kallad tvångslicens har funnits sedan 2001. Då skrev Världshandelsorganisationens medlemmar på Doha-deklarationen. Tvångslicenser ska användas för att ge medborgare tillgång till läkemedel vid ett hot mot folkhälsan, men det är upp till landet själv att avgöra vilka sjukdomar och läkemedel som omfattas.
Tvångslicensering har sedan det tillkom bara använts av ett fåtal länder. Tills förra året, då något började hända. Stora länder som Brasilien, Indien och Kina valde att använda sig av tvångslicenser för en rad hiv- och cancerläkemedel. Något som inte mottagits väl av de patenthållande läkemedelsföretagen. Men än så länge har domstolarna dömt till fördel för generikaföretagen. Senast, i början av mars, fastställde en indisk domstol att tvångslicensen på Bayers njurcancerläkemedel Nexavar fortfarande gäller. Genom tvångslicens har behandlingskostnaden för patienterna kunnat sänkas från 35 000 kronor till drygt tusen kronor per månad.
Anledningen till att tvångslicensering inte använts så mycket är enligt PehrOlov Pehrson, läkare och tidigare ordförande för Läkare utan gränser i Sverige, att det är krångligt tekniskt och osäkert juridiskt.
– Det beror dels på att det är en ovanlig och komplicerad process att använda sig av flexibiliteten i TRIPS-avtalet. Det krävs nästan att landet har en fungerande läkemedelsproduktion för att det ska vara någorlunda smidigt. Till exempel försökte Rwanda få till stånd tillverkning av ett hiv-läkemedel i Kanada enligt tvångslicens, men det tog väldigt lång tid innan det blev möjligt.
– Den andra anledningen är att de länder som har produktionskapacitet, till exempel Indien, har dragits inför domstol av läkemedelsföretagen. De riskerar alltså stora rättegångskostnader, och tänker sig noga för eftersom det är en osäker utgång. Det krävs ett antal fall för att det ska skapas prejudikat. Efter två-tre fall kanske patenthållarna väljer att inte väcka åtal och det kan leda till att generikaproducenterna vågar mer, säger han.
Förklaringen till att det är just Brasilien, Kina och Indien som tagit täten är att de har produktionskapacitet för avancerade läkemedel, vilket de fattigaste länderna inte har. PehrOlov Pehrson tror att det som skett under 2012 är början på en trend.
– Om andra länder ser att det är möjligt och fungerar tror jag att fler kommer att följa efter. I många länder växer det fram en stor inhemsk medelklass som har möjlighet att kräva tillgång till moderna läkemedel och ifrågasätta höga kostnader. Det handlar om informationsspridning också. Oavsett var i världen man befinner sig så vet nu både patienter och läkare att dessa läkemedel finns och då ökar det politiska trycket. Indien har definitivt kommit längst, både vad gäller produktion och export.
Branschföreningen Lif har inte arbetat med frågan om tvångslicenser i någon större omfattning, erkänner vd Anders Blanck. Han menar att läkemedelsbranschen på en övergripande nivå accepterat att fattiga länder i vissa fall har möjlighet att bryta ett patent för att säkra tillgången till läkemedel för den egna befolkningen.
– Konceptet med tvångslicenser har förhandlats fram under lång tid, och industrin har ett ansvar för att det finns tillgång till livsviktiga läkemedel även i fattiga länder. Men frågan om tvångslicenser som sådana är ju självklart ingenting som accepteras utan diskussion, och det kräver ett ställningstagande i varje enskilt fall.
Anders Blanck menar att det finns många sätt att säkerställa tillgången till läkemedel på.
– Den bild jag har är att de länder som hittills använt sig av tvångslicensering kanske inte nödvändigtvis är de fattigaste länderna. Till exempel satsar Thailand stora pengar på uppbyggnad av sin militär, men också på att kunna erbjuda sjukvårdsturister högklassig vård i landet. Är det då rätt att säga att de inte har råd att betala för just läkemedel? Kina kan också diskuteras, då landet är en av världens snabbast växande ekonomier. De har en inhemsk industri, och det kan åtminstone misstänkas att de vill använda den istället för att importera läkemedel.
PehrOlov Pehrson håller inte med eftersom det finns stora ekonomiska skillnader för befolkningen i Brasilien, Indien och Kina.
– Det har hela tiden funnits en vilja hos den forskande läkemedelsindustrin att bara acceptera tvångslicenser för vissa länder och vissa läkemedel. Till exempel var det en stor strid innan man accepterade att hiv-läkemedel omfattas. Vi på Läkare utan gränser tycker inte att det bara handlar om läkemedel för överlevnad utan även om icke-smittsamma sjukdomar, till exempel mot hjärtsjukdomar, diabetes och cancer. Dessa sjukdomar har även blivit vanligare i länder som Indien. Det leder till en intressekonflikt med läkemedelsindustrin, men vi ser det ur patienternas synvinkel. Man kan inte stanna vid akuta sjukdomar. Läkare utan gränser vill inte slopa patenträtten för läkemedelsindustrin, men vi strävar efter tillgång till moderna läkemedel för alla vilket leder till bättre folkhälsa.
Han menar att läkemedelsföretagen bör hitta nya strategier i de länder där tvångslicens genomförts.
– Den forskande läkemedelsindustrin måste hitta andra sätt att förhålla sig till tvångslicenser än att ta fallen till rättegång. När fler länder får tillgång till tekniken för att producera egna läkemedel talar mycket för att de kommer att göra det.
Richard Bergström, vd för den europeiska branschorganisationen Efpia, ser inte tvångslicenser som en lösning på läkemedelstillgången.
– Även om alla läkemedelspatent togs bort i Indien finns det inte tillräckligt med pengar i den indiska hälsobudgeten att förse alla patienter med läkemedel.
– Strategin är att med olika access-program och frivilliga licenser görs så mycket som möjligt för att de som behöver läkemedlen får tillgång till dem. Utmaningen för alla är att se till att de patienter i Indien som är lika rika som i Sverige också respekterar patent och accepterar ett högre pris för att betala för innovation. Denna så kallade "tiered pricing" mellan invånare i ett land är svårt i praktiken, men används exempelvis i Brasilien för nya cancerläkemedel. Med en växande medelklass i länder som Kina, Brasilien och Indien tycker jag det är moraliskt fel om bara vi i Europa och USA skall betala för ny forskning, säger Richard Bergström.
Vaccinerade slapp könsvårtor
Forskare vid Karolinska institutet har följt upp 124 000 flickor och kvinnor i Sverige som någon gång mellan 2006 och 2010 fick det HPV-vaccin som skyddar mot både kondylom och HPV16 och HPV18, alltså Gardasil. De som ingick i studien var mellan 10 och 44 år gamla och har följts upp i snitt i 4,4 år via olika register.
Forskarna undersökte både vaccinets effekt och vilka som vaccinerade sig. Eftersom livmoderhalscancer tar längre tid att utveckla undersöktes inte förekomsten av det. Däremot visade det sig att hos flickor som blivit vaccinerade före 14 års ålder sjönk förekomsten av kondylom med 93 procent. I gruppen som vaccinerade sig efter 20 års ålder var skyddet under 50 procent.
Utbildningsgrad påverkade i hög grad vilka som vaccinerade sig. Det var 15 gånger vanligare att barn till universitetsutbildade föräldrar vaccinerade sig än barn till lågutbildade föräldrar. Om mamman var universitetsutbildad var det åtta gånger vanligare att flickan blev vaccinerad jämfört med fyra gånger vanligare om det var pappan som var universitetsutbildad.
Vaccinering mot HPV ingår sedan 2012 i det allmänna vaccinationsprogrammet. Från 2007 har flickor mellan 13 och 17 år erbjudits vaccination till reducerat pris, medan andra fått betala fullpris.
– Vår studie ger stöd för att vaccinet ska tas vid så låg ålder som möjligt. När vaccineringen erbjöds till rabatterat pris var fördelningen mycket ojämlik. Genom att låta vaccinet vara gratis och erbjudas via skolor kommer fördelningen troligen att bli mer jämlik, säger Lisen Arnheim-Dahlström, forskare vid KI, i ett pressmeddelande.
Studien som är publicerad i Journal of the National Cancer Institute, är finansierad av läkemedelsföretaget MSD, som marknadsför Gardasil. En av forskarna bakom studien är anställd på Sanofi Pasteur MSD.
Det finns idag två vacciner mot humant papillomvirus, Gardasil och Cervarix. Gardasil skyddar även mot kondylom.
Ännu ett dödsfall av nytt coronavirus
Det nya viruset NCoV upptäcktes på den arabiska halvön i somras och sedan dess har 15 personer bekräftats vara smittade, enligt Värdshälsoorganisationen WHO. Nio av dem har dött.
Det senaste fallet var en saudiarabisk man i 39-års åldern. Han blev sjuk den 24 februari, inlagd på sjukhus den 28 februari och avled den 2 mars. Han ska enligt preliminära undersökningar inte ha haft någon kontakt med de tidigare kända fallen, enligt WHO.
Under februari upptäcktes tre nya fall av coronaviruset i Storbritannien. Indexfallet insjuknade efter en resa till Saudiarabien och Pakistan. De andra tillhörde den insjuknades familj och hade varit i nära kontakt med hen.
Mycket talar för att smittan i sällsynta fall kan spridas mellan människor, men enligt Smittskyddsinstitutet är risken att smittan ska spridas utanför den närmaste kretsen runt en sjuk person mycket liten. I Storbritannien och Tyskland har man tagit prov på fler än 200 personer som haft nära kontakt med de aktuella fallen, utan att man sett några tecken på smittspridning.
Stor utveckling av biologiska läkemedel
En ny rapport från branschorganisationen Pharmaceutical Research and Manufacturers of America, PhRMA, visar på en hög aktivitet kring biologiska läkemedel hos amerikanska biopharmaföretag. 907 biologiska läkemedel och vacciner mot över 100 sjukdomar testas i kliniska studier eller granskas av FDA just nu.
Bland dessa läkemedel finns 338 cancerbehandlingar, 134 vacciner mot infektionssjukdomar, 71 behandlingar mot autoimmuna sjukdomar och 58 behandlingar för hjärt-kärlsjukdomar.
Den största delen av forskningen genomförs på monoklonala antikroppar och vacciner, enligt rapporten.
Några av de nya behandlingarna är ett genetiskt modifierat virusbaserat vaccin mot melanom, en monoklonal antikropp mot astma och en antisensbehandling mot leukemi.
Apoteken väljer försäkrade
Förra året såldes omkring 83 miljoner läkemedelsförpackningar i Sverige. Knappt 160 000 av de förpackningarna som byttes var parallellimporterade produkter utanför försäkringen, enligt branschorganisationen Sveriges apoteksförening.
Problemet med att den som anmäler en läkemedelsskada får inte ärendet prövat av Läkemedelsförsäkringen om inte läkemedlet kommer från ett företag som är försäkrat har uppmärksammats i medier den senaste tiden. Det har fått flera företag, bland annat Ranbaxy och KRKA att gå med.
Nu har alla apotek som är anslutna till Apoteksföreningen ingått en överenskommelse att inte ingå avtal med parallellimportörer som inte är anslutna till Läkemedelsförsäkringen.
– Apoteksaktörerna har möjlighet att ställa mer långtgående krav än staten när vi förhandlar med läkemedelsbolagen. Att en del av de läkemedel som säljs i Sverige inte ingår i Läkemedelsförsäkringen har varit ett kvalitetsproblem som apoteken varit obekväma med, säger Johan Wallér, vd för Sveriges apoteksförening, i ett pressmeddelande.
Apoteken har avvaktat en eventuellt statlig reglering av Läkemedelsförsäkringens omfattning och många ställer redan idag krav på parallellimportörerna, men genom överenskommelsen vill apoteksbranschen visa att man tar ett ansvar utöver vad staten kräver.
Anders Öhlén, vd för Läkemedelsförsäkringen, tycker att det är bra att apoteken bidrar där de kan påverka.
– Även om alla parallellimportörer som är anslutna till Läkemedelshandlarna är med i Läkemedelsförsäkringen är det väldigt positivt eftersom överenskommelsen kan förhindra att det kommer in nya parallellimportörer på marknaden som står utanför. Men det löser inte problemet med icke anslutna generikaföretag, säger han till Läkemedelsvärlden.
Inom ramen för generikasystemet byttes förra året drygt två miljoner förpackningar till en vara som stod utanför försäkringen.
Med fokus på läkemedelsforskning
Lilian Walther Jallow har blivit ny vetenskaplig sekreterare vid Apotekarsocietet. I den nya rollen kommer hon att bevaka forskningsfrågor och stärka Apotekarsocietetens engagemang på området, nationellt så väl som internationellt.
– Läkemedelsforskningen världen över är inne i en omvälvande fas med nedläggning av forskningsavdelningarna på många av de stora företagen. Detta innebär svårigheter, men även nya möjligheter för området. I dagens läge behövs extra fokus på läkemedelsforskningen, internationellt och inte minst nationellt, säger hon.
Lilian Walther Jallow arbetar idag som utbildningsledare inom drug discovery vilket hon kommer att fortsätta med. Hon har disputerat vid Karolinska institutet och har forskat kring hiv med fokus på vaccinutveckling. Hon har också initierat testning av hiv på kliniker och blodcentraler i flera afrikanska länder.
Abbvie stämmer EMA
Mitt under diskussionerna om krav på läkemedelsföretagens öppenhet vill företaget Abbvie stoppa EMA från att släppa data om Humira. Humira (adalimumab) används för att behandla bland annat reumatiod artrit och de uppgifter som Abbvie vill skydda är rådata om preparatets effekt och säkerhet.
Enligt Financial Times är det ett annat läkemedelsföretag, UCB, som har vänt sig till EMA för att få ut informationen, något som Abbvie sätter sig emot. Företaget menar att det rör sig om konfidentiella uppgifter och kommersiellt känslig information och bekräftar att man lämnat in en ansökan till EU-domstolen för att hindra EMA att dela med sig av informationen.
Martin Harvey-Allchurch, kommunikationschef på EMA säger till Pharma Times att tre liknande fall väntar på svar i domstolen, ytterligare ett från Abbvie och ett från företaget Intermune.
– Vi kommer att fortsätta att svara på och behandla alla förfrågningar om data tills des att domstolen säger annat, säger Martin Harvey-Allchurch.
Abbvie bildades vid årsskiftet när företaget Abbott delades upp i två.
Granskning av domperidon
Redan 2011 rekommenderade den europeiska läkemedelsmyndigheten EMA att produktinformationen för domperidon skulle uppdateras. Detta för att informera om uppmärksammade biverkningar som hjärtpåverkan och rytmrubbningar. Sedan dess har nya rapporter om liknande biverkningar kommit i Belgien och belgiska myndigheter har nu föreslagit att domperidon inte ska användas av vissa patienter med hjärtproblem.
EMAs säkerhetskommitté, PRAC, kommer nu att inleda en granskning och ntvärdering av de data som finns om läkemedlet för att ta ställning till hur det ska används inom EU.
Domperidon är en dopaminantagonist som påverkar tarmrörligheten och används för att lindra kräkningar, illamående och obehag och sura uppstötningar från buken. Enligt Socialstyrelsens statistik var det 595 personer som använde läkemedlet i Sverige under 2012. De patienter som behandlas uppmanas av Läkemedelsverket att vända sig till behandlande läkare med eventuella frågor.
TLV administrerar glesbygdspengar
För att hela landet ska försäkras en bra läkemedelsförsörjning har regeringen beslutat om ett statsbidrag för att stödja de som annars kan ha svårt att gå runt. I budgeten finns sedan tidigare 20 miljoner avsatta som glesbygdsstöd.
För att få del av pengarna ska ett apotek under kalenderåret som föregått bidragsåret ligga minst tjugo kilometer från ett annat öppenvårdsapotek. Butiken ska vara öppen alla kalendermånader och man ska ha haft intäkter på minst en miljon kronor men inte mer än tio miljoner kronor.