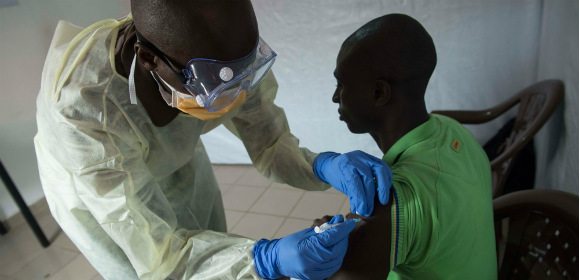
En bråkdel av de barn som drabbas av cancer får vård utomlands. Av de totalt 1 900 barn som de senaste fem åren har behandlats på något av Sveriges sex barncancercentrum har cirka 40 rest utomlands för vård, behandling eller studier. Det visar en kartläggning i Barncancerfondens årsrapport, som släpps i dag, tisdag.
Det kan handla om etablerade metoder som inte används i Sverige eller som används mycket sällan. Det handlar också om barn vars föräldrar söker icke etablerade, experimentella behandlingar utomlands för sina svårt sjuka barn i de fall där den etablerade cancervården inte har mer att erbjuda. Enligt kartläggningen, som är den första i sitt slag, har mellan 10 och 15 barn fått experimentell behandling som det i nuläget saknas vetenskapliga belägg för.
Enligt Anders Castor, sektionschef vid barncancercentrum i Lund har intresset för att söka vård utomlands ökat.
– De här föräldrarna befinner sig i en mycket svår sits. De vill göra allt de kan för sitt barn och hoppas att det kanske ligger en bot där ute och väntar. Jag upplever att det är fler som diskuterar och funderar på att söka vård utomlands i dag, även om det verkliga antalet inte har ökat, säger Anders Castor, i anslutning till Barncancerfondens rapport.
Särskilt stor uppmärksamhet har behandlingar vid ett sjukhus i Monterrey i Mexiko fått. Bland annat har föräldrar till barn med den aggressiva hjärntumören ponsgliom samlat in pengar, i vissa fall upp till flera miljoner kronor, för en experimentell behandling vid sjukhuset.
Ponsgliom är en ytterst aggressiv hjärntumör som drabbar ungefär åtta svenska barn om året. I dag saknas bot. Strålning kan få tumören att krympa tillfälligtvis, men de barn som drabbas överlever sällan längre än två år efter diagnos.
Kliniken i Mexiko och de behandlande läkarna har dock inte redovisat någon vetenskaplig dokumentation kring verksamheten vilket gör det omöjligt att veta exakt vilken behandling som ges. Hittills finns heller inga belägg för att behandlingarna haft någon dokumenterat långsiktig positiv effekt.
– Barncancerfonden anser att nya och oprövade behandlingar bör göras som en del i kliniska studier. Då finns alla tillstånd på plats, etiken kan säkerställas och vi kan bygga kunskap för framtida sjuka barn. Samtidigt har jag full förståelse för att man som drabbad förälder tar varje liten möjlighet som man tror kan rädda ens barn, säger Kerstin Sollebrant, forskningschef på Barncancerfonden.
I ett reportage på KIT.se beskrivs behandlingarna vid kliniken i Monterrey som individanpassade cytostatikablandningar kombinerat med immunterapi. Men i vilka kombinationer och i vilka doser är inte känt. På klinikens egen hemsida finns mycket knapphändig information om behandlingen som beskrivs som ”intra arteriell”, det vill säga att läkemedlen ges i direkt anslutning till tumören.
Frågan om de experimentella behandlingarna diskuteras inte bara i Sverige. Enligt The Daily Telegraph ska en australisk hjärnforskare, expert på hjärntumörer, resa till kliniken i Monterrey för att på plats undersöka verksamheten sedan flera australiska föräldrar tagit sina barn till kliniken för behandling. Resan finansieras av organisationen The cure brain cancer foundation (CBCF).
I Barncancerfondens rapport framgår även att ungefär tio svenska barn har deltagit i godkända kliniska studier de senaste fem åren. I dag finns två kliniska prövningscentrum i Sverige, ett i Stockholm och ett i Göteborg, för barn med cancer vilket möjliggör deltagande i klinisk forskning i Europa. För ett år sedan behandlades det första svenska barnet med ponsgliom i en internationell klinisk studie i Frankrike, något som Läkemedelsvärlden.se skrev om då.
Kerstin Sollerbrant betonar vikten av att Sverige nu kan medverka i internationella kliniska studier.
– Det ökar möjligheterna för barn att delta i kliniska studier även här, vilket kommer att bidra till bättre behandlingar och på sikt ökad överlevnad. Forskning är vägen framåt, säger Kerstin Sollerbrant.