Vid sitt senaste möte rekommenderade den europeiska läkemedelsmyndighetens vetenskapliga kommitté CHMP godkännande för sex nya läkemedel.
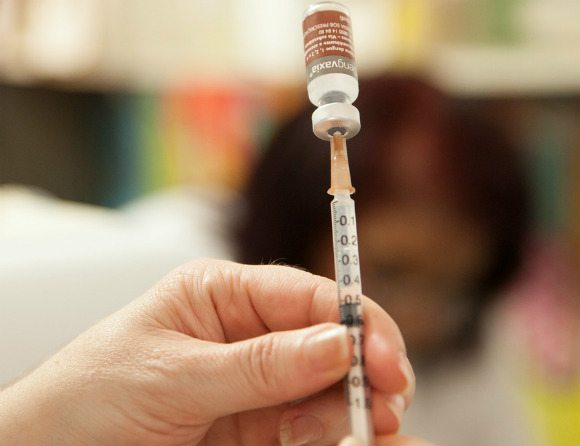
Bland dem finns denguevaccinet Dengvaxia, som om det godkänns, blir det första vaccinet mot denguefeber i Europa. Vaccinet är sedan tidigare godkänt i ett tiotal tropiska länder där denguefeber är vanligt förekommande.
Den nu rekommenderade indikationen undantar dock de stora delar av EU som inte har tropiskt klimat, och där sjukdomen alltså inte finns, och inkluderar bara de områden är sjukdomen finns endemiskt.
Vaccinet är godkänt för barn och vuxna mellan 9 och 45 år och som haft minst en dengueinfektion tidigare. Denguefeber orsakas av ett virus och vaccinet skyddar mot serotyperna 1, 2, 3 och 4.
Första godkännandet för Dengvaxia kom i Mexiko 2016, men vid uppföljningsstudier visade det sig att personer som inte haft denguefeber innan de fick vaccinet riskerade att utveckla en allvarligare form av sjukdomen om de smittades av viruset efter vaccinationstillfället, något som Läkemedelsvärlden rapporterat om.
Bolaget bakom Dengvaxia, Sanofi, uppdaterade därefter informationen till bland annat förskrivare och myndigheter om att vaccinet endast ska ges till personer som redan blivit smittade med minst en serotyp av viruset.
I CHMP:s rekommenderade godkännande fastslås också att laboratorietest ska användas för att bekräfta tidigare smitta innan vaccinet ges.
Under sitt oktobermöte gav CHMP även tummen upp för en ny monoklonal antikroppsbehandling, Takhzyro (lanadelumab), av den ovanliga sjukdomen hereditärt angioödem (HAE). Sjukdomen beräknas drabba färre än en halv på 10 000 personer och visar sig som anfallsvisa svullnader i slemhinnorna i alla delar av kroppen. Tillståndet är potentiellt livsfarligt om till exempel slemhinnorna runt struphuvudet svullnar upp, vilket kan förhindra andningen.
Läkemedlet, som klassas som ett särläkemedel och rekommenderas godkännande för HAE-patienter från 12 år och uppåt, känner igen och attackerar ett visst protein vilket därmed påverkar en händelsekedja som innebär färre angioödemattacker.
Antikroppen ges via subkutana injektioner varannan till var fjärde vecka, vilket enligt CHMP är en fördel jämfört med dagens behandlingar som antingen ges intravenöst eller med tätare intervall med subkutana injektioner. De vanligaste biverkningarna var reaktioner vid injektionsstället.
Ytterligare ett särläkemedel fick positiv bedömning vd oktobermötet. Namuscla (mexiletinhydroklorid) är den första behandlingen för den ovanlig sjukdomen non-dystrofia myotonika. Sjukdomen består av flera undergrupper men gemensamt för dem alla är att de är ärftliga muskelsjukdomar där musklerna har svårt att slappna av efter kontraktion. De livslånga besvären yttrar sig bland annat som smärta, trötthet och muskelstelhet.
Sjukdomen orsakas av felaktigheter i muskelcellernas jonkanaler, vilket leder till att passagen av bland annat natrium och kalium inte blir optimal. Natirum och kalium har en central roll i musklernas kontraktion och avslappning.
Substansen mexiletin, som länge använts för att återställa normal hjärtrytm, godkändes i Europa redan på 1970-talet. Det verkar genom att blockera jonkanalerna för natrium in i muskelcellerna och därmed bidra till att musklerna slappnar av.
Det nu rekommenderade godkännandet av mexiletin för behandling av dystrofia myotonika bygger på data från en fas III-studie med patienter med non-dystrofia myotonika, samt data i litteraturen. Resultaten visar att behandling med mexiletin gav mindre muskelstelhet hos patienterna.
De vanligaste biverkningarna var halsbränna, illamående, kräkning, diarré och magsmärtor. En annan, mindre vanlig biverkan, var arytmi och i rekommendationen anger därför CHMP att kontroller med bland annat hjärtmonitorering bör göras vid behandling. Läkemedlet rekommenderas godkännande för behandling av vuxna patienter.
Kommittén rekommenderade även godkännande för influensavaccinet Flucelvax tetra, ett fyravanlent vaccin för förebyggande av säsongsinfluensa hos barn och vuxna från nio år och uppåt. Även ett läkemedel för underhållsbehandling av kronisk obstruktiv lungsjukdom, KOL, fick tummen upp, liksom biosimilaren Ogivri (trastuzumab) för behandling av bröst och magcancer.
Under oktobermötet valdes dessutom Bruno Sepodes till ny vice ordförande för CHMP. Bruno Sepodes kommer från Portugal och efterträder Harald Enzmann, som vid septembermötet valdes till ny ordförande för CHMP efter Tomas Salmonson, som lämnade posten efter sex år.