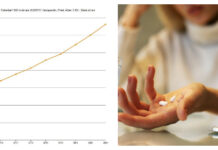
Totalt tog Läkemedelsverket emot 8 465 anmälningar om misstänkta läkemedelsbiverkningar förra året. Det är 379 fler än 2015 då 8 086 tags emot, vilket framgår i verkets biverkningsrapport för 2016.
De flesta rapporterna, drygt 75 procent, kom från hälso- och sjukvården och resten från patienter och konsumenter. Flest anmälningar från hälso- och sjukvården gällde substanserna warfarin, apixban och rivaroxban och den vanligaste rapporterade allvarliga biverkningen gällde blödning – vilket är en känd biverkning med dessa blodförtunnande läkemedel.
Näst vanligast var biverkningar rörande intoxikation och förgiftning av paracetamol. Dessa rapporter kom till stor del från Giftinformationscentralen och rörde i majoriteten av fallen avsiktlig överdosering av paracetamoltabletter med förlängd frisättning. Den europeiska läkemedelsmyndighetens säkerhetskommitté PRAC genomför på initiativ av Läkemedelsverket en granskning av denna form av paracetamol och rapporten väntas bli klar i sommar.
Från privatpersoner gällde de flesta biverkningsanmälningarna substansen levotyroxin, som används för behandling av hypotyreos, och hormonspiral med gestagen. För levotyroxin var de vanligaste inrapporterade biverkningarna trötthet, bristande effekt och viktökning medan det för hormonspiralen var buksmärtor och nedstämdhet. Gällande allvarliga biverkningar rapporterades för de senare 31 fall av oönskad graviditet och 21 fall av utomkvedshavandeskap.
Generellt rörde de inrapporterade biverkningarna kvinnor i högre grad än män, 60 procent jämfört med 40 procent. Även bland hälso- och sjukvårdens anmälningar om allvarliga biverkningar dominerade kvinnorna där de vanligaste anmälningarna var kopplade till avvikelser vid behandling av nervsystemrelaterade besvär. Enbart biverkningar rörande njur- och urinrelaterade besvär var något vanligare hos män.
Läkemedelsverket skriver i sin rapport att värdet av inrapporterade biverkningar är mycket stort då de kan bidra till att hitta tidiga signaler på ännu inte noterade biverkningar. Vid kliniska prövningar och senare lansering av ett läkemedel är en stor del av biverkningarna kända, men när läkemedlet börjar användas i stor skala under en längre tid i en bredare och mindre homogen patientgrupp kan andra, dittills okända, biverkningar ge sig till känna. Läkemedelsverket vill dock att fler misstänkta biverkningar ska rapporteras.
– Det är positivt att vi ser att misstänkta biverkningar rapporteras till Läkemedelsverket för utredning i ökande grad men samtidigt vet vi att det finns en stor underrapportering. Det är särskilt viktigt att man rapporterar in allvarliga eller okända biverkningar, säger Kerstin Jansson, enhetschef på Läkemedelsverket, i en kommentar till rapporten.