I takt med att antalet dödsfall orsakade av opioid-överdoser ökat kraftigt i USA de senaste åren, har även behovet av skedeminimerande insatser ökat. Liksom i Sverige är förbättrad tillgång till motmedlet Naloxon en av hörnstenarna i arbetet.
Till skillnad från i Sverige kan även icke utbildad vårdpersonal, det vill säga allmänheten, i ett antal stater ge Naloxon till personer som överdoserat med exempelvis heroin eller opioidläkemedel. Kunskapen om vilket administreringssätt som fungerar bäst vid en bredare användning är dock låg.
Amerikanska forskare har därför undersökt effekten av olika administreringsformer av Naloxon när motmedlet ges av allmänheten.
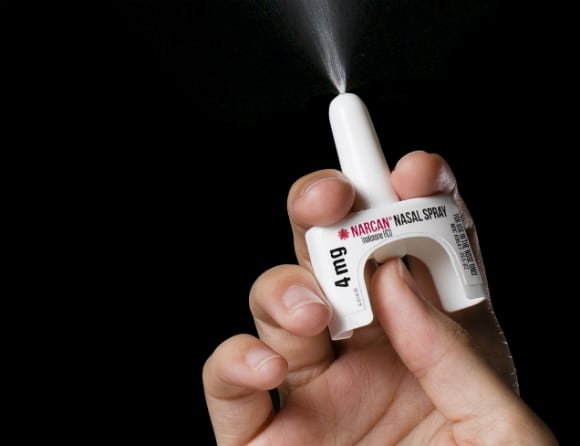
Studien, som är publicerad i tidskriften Addiction, visar att administrering av Naloxon via nässprej var mest framgångsrik gällande hur många som lyckades ge läkemedlet korrekt och hur snabbt man lyckades ge det.
Totalt medverkade 138 personer, samtliga över 18 år, i studien. De medverkande randomiserades till tre lika stora grupper och fick ge Naloxonsimulerande behandling som enkeldos via nässprej, som nässprej med ett automatiserat flerstegsförfarande eller som intramuskulär injektion.
Resultaten visar att andelen som lyckades ge behandlingen korrekt skilde sig åt mellan grupperna. Medan samtliga i gruppen som gav enkeldos nässprej lyckades administrera läkemedlet framgångsrikt var det endast 70 procent i gruppen som gav intramuskulär injektion som lyckades. Skillnaden var statistiskt signifikant.
Även gruppen som gav nässprejen i flera steg var mer framgångsrik än injektionsgruppen, 89 procent jämfört med 70 procent lyckades, men den skillnaden var inte statistiskt säkerställd.
Av de 119 studiedeltagare som gav det Naloxonliknande medlet framgångsrikt tog det signifikant kortast tid för de i nässprejsgruppen – 34 sekunder, jämfört med 100 och 110 sekunder för injektionsgruppen respektive gruppen med flerstegs-nässprejen.
Studiedeltagarna gav behandlingen till provdockor och studien genomfördes på en publik plats i USA med stor folkgenomströmning, för att simulera så verkliga förhållanden som möjligt.
Innan interventionen fick studiedeltagarna, var och en för sig, se en två minuter lång introduktionsvideo om det administreringssätt man randomiserats till. Inga frågor fick ställas till studieledarna vare sig under videon eller i samband med den efterföljande läkemedelsadministreringen.
Studiedeltagarnas agerande observerades och dokumenterades under hela studietiden, och utvärderades utifrån ett antal på förhand uppställda kriterier.
Forskarna bakom studien pekar på flera svagheter med studien, främst att den genomfördes på dockor och med ett Naloxonsimulerande medel. Det är därför möjligt att resultaten inte till fullo speglar en verklig situation, menar de.
I studien undersöktes heller inte intramuskulär Naloxon med autoinjektor, som tidigare visat goda resultat på framgångsrik administrering. Anledningen är enligt författarna att denna form är väsentligt dyrare än övriga Naloxon-former, och därför sannolikt inte kommer att prioriteras i allmänna Naloxon-program.
Forskarna konstaterar dock att sedan studien genomfördes 2016 har möjligheterna för allmänheten att köpa Naloxon utan recept, och eventuellt utan användarinstruktioner, ökat markant, och att studien därför ger värdefull information om vilken typ av administreringsform allmänheten kan förväntas behärska bäst.
I Sverige kan sedan tidigare i år Naloxon förskrivas av sjuksköterskor och motmedlet får, förutom av hälso- och sjukvårdspersonal, även ges av räddningspersonal i väntan på ambulans, något som Läkemedelsvärlden skrivit om tidigare.